Definisjon
Mikroskopisk polyangiitt (MPA) er en vaskulitt-sykdom tilhører ANCA-vaskulittene. Den er dermed beslektet med GPA/Wegeners granulomatose og EGPA/Churg-Strauss vaskulitt. Mikroskopisk polyangiitt angriper små blodårer i ulike organer, og spesielt er nyrene utsatt (nekrotiserende glomerulonefritt), noe som ubehandlet fører til alvorlig nyresvikt. Også andre organer som lunger, hud, mage-tam og nerver kan skades i sykdomsforløpet (referanse: Jeanette JC, 2013). De fleste har spor av blod og proteiner i urinen, noe som undersøkes via urinprøve. Antistoff-prøven MPO-ANCA er typisk i blodet. Nyrespesialister (nefrologer) og revmatologer samarbeider ofte om utredning og behandling. Det finnes effektive legemidler som stanser sykdommen i de aller fleste tilfellene (referanse: EULAR: Yates M, 2016).
Historie
Mikroskopisk Polyangiitt (MPA) var tidligere antatt å være en type polyarteritis nodosa (PAN) og ble forslått som separat diagnose først i 1985 (referanse: Savage C, 1985). Senere har oppdagelsen av ANCA og genetiske markører underbygget at MPA er en egen sykdom.
Forekomst
Mikroskopisk Polyangiitt (MPA) er en sjelden sykdom, men den forekommer over hele verden. Vanligste alder ved sykdomsstart er 64-74 år. Den er svært uvanlig blant barn. Menn angripes litt yppigere enn kvinner (1,8:1). Forekomsten varierer mellom ulike studier. Antall nye tilfeller årlig pr million person-år på verdensbasis er MPA: 5,9 (4,9-16) (Redondo-Rodriguez R, 2022; Berti A, 2017). I Norge og Sverige er forekomsten beregnet til henholdsvis 2,7 og 10,1 nye tilfeller / million innbyggere årlig (insidens), noe som tilsvarer ca. 14-54 nye tilfeller årlig i Norge (referanser: Watts R, 2001; Mohammad AJ, 2009). Forekomsten (insidens) i i Europa og USA er i de fleste studier er omtrent som ved GPA / Wegeners granulomatose. I Asia er imidlertid MPA klart vanligere (referanse: Fujimoto S, 2006). Antall personer som har MPA på et bestemt tidspunkt (prevalens) er beregnet til 94/million i en svensk studie, noe som tilsvarer ca. 500 personer i Norge. Prevalensen er da lavere enn for GPA / Wegeners granulomatose (160/million) (referanser: Mohammad AJ, 2007; Watts RA, 2012). Årsaker til lik insidens, men lavere prevalens av MPA sammenlignet med GPA er sannsynligvis at MPA varer kortere/er mindre kronisk.
Sykdomsårsak
Sykdomsårsaken er fortsatt ukjent, men en disposisjon kan foreligge gjennom arveanlegg (gener) og miljøfaktorer. I de aller fleste tilfellene kan en ikke peke på en spesiell utløsende årsak. Genetikk: Mikroskopisk polyangiitt (MPA) er ikke spesielt arvelig, men noen gener (HLA-DQ-gener) er i forsknings-studier funnet å disponere. Disse er med på å skille MPA fra Granulomatøs Polyangiitt (GPA) som assosieres med HLA-DP -assosiasjon. De fleste med disse arveanleggene blir likevel ikke syke og ingen arvelig disposisjon undersøkes i vanlig utredning eller oppfølgingen av sykdommen (referanse: Millet A, 2013). Medikamenter og rusmidler: Propetyluracil brukes mot Graves sykdom (hyperthyreose / høyt stoffskifte) kan en sjelden gang utløse ANCA-vaskulitt. Vanligste bivirkning av propetyluracil er imidlertid agranulocytose (lavt antall granulocytter i blod) (referanse; Lillejordet E, 2019). Hydralasin (tidligere brukt mot høyt blodtrykk), minocyclin (et antibiotikum), allopurinol (mot urinsyregikt) og rifampicin (mot tuberkulose) er andre medikamenter som mistenkes å kunne utløse MPA.
Sykdomsutvikling / patogenese
Når sykdommen først har begynt, dannes revmatisk betennelse (inflammasjon, uten infeksjon) i blodåreveggene. Oftest angripes kapillærer, venuler og arterioler som er de minste blodårene vi har. Prosessen resulterer i at celler dør (nekrose). I nyrene skades også nyrevevet (glomeruli), slik at normalt vev dør og erstattes med bindevev i form av fibrin (fibrinoid nekrose). Ved MPA ses ikke granulomer, til forskjell fra GPA og EGPA.
Symptomer
Allmennsymptomer merkes først, mens organ-manifestasjon i form av nyrebetennelse (glomerulonefritt) som er mest typisk, kommer senere. Tidlige symptomer er ny tretthet (hos nær 100%), nattesvette (70%) og feber uten annen forklaring (40%). Tidlige symptomer er dermed lite karakteristiske, noe som medfører at sykdommen ofte gjenkjennes først etter flere måneders forløp (referanse: Agard C, 2003).
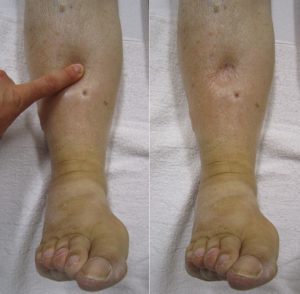
Nyrer. Noen observerer at urinen skummer ved vannlating. Karakteristiske symptomer på nyrebetennelse og nyresvikt er sene manifestasjoner som merkes ved økt væske i vevet (ødem) i begge bena eller hevelse rundt øyne / i ansiktet som kan være del av et «nefrotisk syndrom» (se nedenfor) (referanse: Chung SA, 2010).
Hud. Symptomer med smerte fra huden oppstår hos ca. 25% (referanse: Kluger N, 2008). Vaskulitt med småprikket utslett (palpabel purpura) er vanligst og ses hos 1 av 3 (>30%). Andre hud-manifestasjoner er livedo retikularis, elveblest (urticaria) og nekroser (dødt vev).
Ledd og Muskler. Leddsmerter (artralgi) og muskelsmerter (myalgi) er vanlig ved MPA og kan forutgå andre symptomer. Imidlertid er både ledd- og muskelsmerter såpass vanlige både i befolkningen generelt og ved mange tilstander at en sjelden vurderer MPA som årsak. Artritt (leddbetennelser) med hevelser i ledd er sjelden og mer typisk for leddsykdommer.
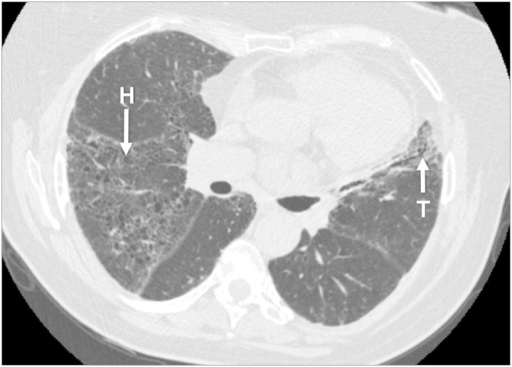
Lunger angripes hos 25-55% (referanse: Chung SA, 2010). Symptomer på lungefibrose kommer svært gradvis og er vanskelig å oppdage tidlig. Lungefibrose kan innebære økende tørr-hoste og tung pust ved belastning, men merkes ikke alltid før tilstanden er kommet langt. Symptomene skyldes at bindevev (fibrose) gradvis erstatter normalt lungevev som følge av gjennomgåtte mindre blødninger (se nedenfor), en direkte fibroserende virkning av MPO-ANCA antistoff eller skade etter revmatisk betennelse i lungene. Lungeblødning på grunn av betennelse i små blodårer (kapillaritt) er en sjelden komplikasjon, men vil raskt medføre puste-vansker, hoste med spor av blod og mindre blødninger. Lungeblødning er alltid alvorlig og massiv lungeblødning er livstruende. Pleuritt er uvanlig betennelse i lungehinnen som typisk medfører brystsmerter ved pusting (referanse: Labadidi MH, 2015).
Mage-Tarm (gastrointestinalt). Smerter i mageområdet forekommer hos ca. 50% (referanse: Pagoux C, 2005). Flere årsaker er mulig. Sår i mage og tarm kan medføre smerter og blødninger. Små blødninger er vanligst. Små aneurismer (utposninger) på blodårer til tarmen kan blø og redusere blodtilførselen (iskemi) (redusert blodtilførsel). Perforasjon av tarmveggen («sprukket mage/tarm) er sjelden.
Nerver. Nervesystemet påvirkes hos 37-72%. Nerver i armer og ben (perifere nervesystem) angripes vanligst: Mononevropati (mononevritt) med nummenhet og redusert følelse i deler av ben eller arm (sensorisk nevropati, mononevritis multiplex, asymmetrisk polynevropati). Polynevropati medfører ganske like symptomer i begge ben eller armer (symmetrisk manifestasjon). Sjeldnere er tap av muskelkraft, men må behandles raskt for å hindre varig skade. Hjernen (sentralnevesystemet, CNS) angripes sjelden, men slag (blødning eller hjerneinfarkt) og pachymeningitt er observert (referanse: Kono H, 2000).
Øyne. Øye-manifestasjoner er vanligvis ikke hovedproblemet ved MPA. Men ved systematisk undersøkelse kan en finne at omtrent 25% får betennelse i øyne i form av episkleritt som gir ømhet og rødhet (referanse: Hara A, 2005).
Undersøkelser
Sykehistorien kan omfatte generell sykdomsfølelse med appetittløshet, ny nattesvette, feber eller tydelig vekttap med flere kg. Symptomer fra nyrene med hevelse i bena eller rundt øynene etterspørres. Hudforandringer, leddsmerter, nerve-symptomer, hoste eller pustevansker og andre symptomer (se ovenfor) styrker mistanken om MPA eller lignende tilstand. Påfallende nese- eller bihule-tetthet er mer typsik for GPA og astma/allergi for EGPA.
Klinisk undersøkelse vurderer øyne, lunger, huden, ledd, nerver, blodtrykk, vekt og om tegn på nyresvikt (hevelser) forelligger.
Blodprøver. Som tegn på revmatisk betennelse (inflammasjon) forventes høy senkningsreaksjon (SR) og CRP. Kreatinin og eGFR gjenspeiler nyrefunksjonen. Albumin kan ved lave verdier tyde på proteintap ved nyre-betennelse / glomerulonefritt. ANCA (immunologiske tester).
Typisk for sykdommen er utslag i antistoffet MPO-ANCA (til stede hos 90% med aktiv sykdom). Ved MPO-ANCA antistoff og symptomer, bør en følge opp med kontroller av blant annet urin og blod en tid fremover for å kunne påvise sykdommen i en tidlig fase. MPO-ANCA antistoff ses også når sykdommen er begrenset til nyrene (renal limited disease). Også ved andre sykdommer påvises MPO-ANCA antistoff (ved EGPA ses MPO-ANCA hos 30-40%, ved Anti-GBM / Goodpastures syndrom med lunge og nyre-manifestasjoner ses MPO-ANCA i 10-40% og GPA har MPO-ANCA i 10-20% av tilfellene).
Urinprøve er alltid viktig for å påvise tidlige tegn til nyrebetennelse. Spor av blod (hematuri) og proteiner/eggehvite kan sjekkes ved stiks på et hvert legekontor. Synlig blod i urinen er uvanlig, men noen kan merke at urinen skummer fordi den inneholder mye protein. Urin-undersøkelse under mikroskop kan vise sylinder-formede celle-aggregater.
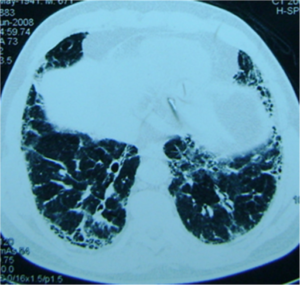
Bildediagnostikk. CT-undersøkelser av lungene vil kunne avdekke tegn til lungefibrose allerede tidlig i forløpet, sjeldnere lungehinnebetennelse (pleuritt) eller blødninger. Vanlig røntgenundersøkelse er ikke tilstrekkelig nøyaktig i denne sammenheng. Tette bihuler (ved CT eller MR-undersøkelse) er ikke typisk for MPA, men vanlig ved GPA/Wegeners.
Vevsprøve (biopsi) er alltid viktig der det er mulig for å sikre diagnosen. Oftest tas vevsprøven fra nyrene (se nedenfor). Hudbiopsi viser oftest «leukocytoklastisk vaskulitt» som bekrefter at forandringene er en type vaskulitt, men disses ses også ved mange andre sykdommer. Granulomer er ikke typisk for GPA (i motsetning til GPA/Wegeners, EGPA/Churg-Strauss, sarkoidose og infeksjoner). Vennligst les mer om nyrebiopsi nedenfor.
Nyrene ved MPA
Nyrene angripes i form av glomerulonefritt hos nesten 100%, ofte allerede når diagnosen stilles. Hvis behandling uteblir, vil tapet av protein medføre for lavt protein (albumin) i blodet og hevelser (vennligst se «nefrotisk syndrom» nedenfor). Etter hvert vil nyrefunksjonen svekkes raskt, noe som påvises i blodprøver. Alvorlig nyresvikt ved diagnosen eller kort tid senere medfører behov for dialyse hos ca. 20% eller flere. Tidlig behandling antas å være avgjørende for å hindre varig nyresvikt. Blant pasienter med behov for dialyse og dårlig prognose for nyrene, er det vist at ca. 14% likevel gjenvinner nyrefunksjonen på sikt (referanse: Lee T, 2014). Nyrebiopsi (vevsprøve fra nyre): Vennligst se avsnitt nedenfor.
–Nefrotisk syndrom. Total protein-utskillelse. mer enn 3 gram/d, + ødemer og lavt albumin i blodet. Manifest glomerulær nyre-sykdom: PK (protein/kreatinin) ratio mer enn 300.
- Normal proteinuri: opptil 150 mg/døgn
- Proteinuri mellom 30-300 mg/døgn regnes som mikro-albuminuri (negativ u-stiks)
- Patologisk proteinuri 300-500 mg/døgn
- Urin-stiks måler albuminuri pr liter:
- 1+ tilsvarer 300-1000 mg/liter
- 2+ tilsvarer 1000-3000 mg/liter
- 3+ tilsvarer > 3000 mg/liter
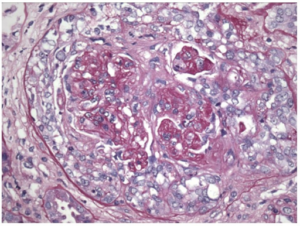
Vevsprøve (biopsi) fra en nyre er viktig for å sikre diagnosen, påvise graden av nyrebetennelse og velge best behandling. Nyrebiopsi viser oftest celleskader i form av «nekrotiserende glomerulonefritt med halvmåne-dannelse og fokal glomerulonefritt». Ved begrenset (fokal glomerulonefritt) er mindre enn 50% av glomeruli er angrepet). Begrepet «halvmåner» henspiller på formasjonen som bindevevet av fibrin danner i nyre-glomeruli initialt. Ved fremskreden sykdom ses mange angrepne nyre-glomeruli og etablerte skader, noe som er av betydning for prognosen og dermed valg av behandling. Resultatet av nyrebiopsi kan likevel ikke skille mellom MPA og GPA vanligvis. Ved immunhistologisk undersøkelse av vevet påvises oftest ikke immunkomplekser, slik som ved Lupus-nefritt eller nedslag av IgA som ved Henoch-Schönlein vaskulitt/IgA-vaskulitt. Granulomatøs betennelse/granulomer er ikke typisk for MPA, men ses ved GPA / Wegeners granulomatose og EGPA (Churg-Strauss vaskulitt). -Den vanligste komplikasjon ved nyrebiopsi er blødning som ses hos 2,2% (referanse: Lees JS, 2017). -Kontra-indikasjoner som gjør at nyre-biopsi ikke skal gjøres (referanse: Bandari J, 2016): Kjent økt risiko for blødning, ukontrollert høyt blodtrykk (systolisk over 160 mmHg), bare en nyre.
Vevsprøve fra hudforandringer viser ofte ”leukocytoklastisk vaskulitt” som også forekommer ved flere andre vaskulitt-sykdommer. Muskelvev kan vise vaskulitt-forandringer (referanse: Nunokawa T, 2016).
Diagnosen
Avgjørende for diagnosen er aktuelle symptomer fra ulike organer (se ovenfor) kombinert med blodprøveutslag (MPO-ANCA antistoff). Typiske forandringer i vevsprøve som oftest tas fra en nyre og viser «pauci-immun /fokal nekrotiserende glomerulonefritt med halvmåner» styrker diagnosen.
Pulmo-renalt syndrom
Med pulmo-renalt syndrom menes at både lunger og nyrer er angrepet. Andre årsaker til pulmo-renalt syndrom er systemisk Lupus (SLE) og Goodpastures syndrom (Anti-basalmembran sykdom).
Klassifikasjonskriterier
ACR / EULAR klassifikasjonskriterier for MPA, (referanse: Suppiah R, 2022)
Kriteriene brukes til å påvise MPA der det foreligger vaskulitt i små og mellomstore kar. Summen av skår ≥ 5 kreves for MPA-diagnosen. Negative tall indikerer at andre diagnoser (GPA eller EGPA) er mer sannsynlig.
| Kliniske kriterier | |
| Nasal manifestasjon: Blodig sekresjon, sår, skorper, fortetninger, blokade eller septumdefekt/perforasjon | -3 |
| Laboratorium-, bildediagnostikk- og biopsi-kriterier | |
| Positive tester for pANCA eller MPO-ANCA | +6 |
| Fibrose eller interstitiell lungesykdom (ILD) ved bildediagnostikk | +3 |
| Glomerulonefritt (Pauci-immun type ihht biopsi) | +3 |
| Positiv test for cANCA eller PR3-ANCA | -1 |
| Eosinofile i blod ≥1 x 109/liter | -4 |
Chapel Hill kriterier
Ofte brukes Chapel Hill concensus kriterier (1994, biopsi-basert) for MPA:
- Biopsi-verifisert nekrotiserende vaskulitt i små kar
- og/eller
- Glomerulonefritt med få eller ingen immunnedslag
- Affeksjon av mer enn ett organsystem, påvist ved biopsi med vaskulitt i små-mellomstore kar eller surrogat parameter for glomerulonefritt
- og
- Fravær av histologisk granulomatøs inflammasjon i respirasjons-tractus
I ettertid er MPO-ANCA antistoff kommet som aktuell markør. Utslag bør vektlegges.
Lignende tilstander/differensialdiagnoser
Det kan være vanskelig å skille mellom de ulike ANCA-vaskulitter (GPA/Wegeners, Mikroskopisk polyangiitt, MPA og EGPA/Churg-Strauss) og Polyarteritis nodosa (PAN) tidlig i forløpet. Mange symptomer overlapper som påvirket allmenntilstand, ledd-, nyre-, lunge- og hud-symptomer. Noen forskjeller kan en merke seg: 1) GPA angriper medfører nesten alltid symptomer fra øvre luftveier (bihuler, nese, ører, luftrør) og PR3-antistoff foreligger i blodet hos de aller fleste med aktiv sykdom. Nyre-manifestasjon er vanlig. 2) MPA har oftest raskt økende nyre-manifestasjon (glomerulonefritt), MPO-ANCA antistoff i blodet hos de fleste og vevsprøve viser glomerulonefritt, men ikke granulomatøs betennelse. 3) EGPA har astma eller KOLS med økende symptomer fra lunger. MPO-ANCA påvises hos omtrent 50%, mens PR3-ANCA er mer uvanlig. 4) PAN kan gi sterke muskelsmerter. Ingen utslag i ANCA i blodet. ANCA-vaskulitter kan iblant forveksles med andre sykdommer (differensialdiagnoser). For andre differensial-diagnoser vises til separat side.
Sykdomsaktivitet og Sykdomsskade
Sykdomsaktivitet ved ANCA-vaskulitt bestemmes på bakgrunn av systemisk betennelse (inflammasjon) og pågående sykdom i organer. ANCA har også en viss betydning, fordi økende ANCA øker risikoen for sykdomsresidiv (referanse: Kemna MJ, 2015). Man kan kalkulere sykdomsaktivitet ved Birmingham Vasculitis Activity Score (BVAS): Alle registrerte parametere i BVAS skal være forårsaket av aktiv ANCA-vaskulitt, ikke infeksjon eller varig skade av sykdommen. Tegn på aktiv sykdom skal være nye symptomer eller forverring i løpet av de siste tre måneder (alternativ er “persisterende sykdom”). BVAS er inndelt i grupper som dekker ni organsystemer. Parametere som registreres skal vurderes for behandling (“intention-to treat”). Kalkulator for BVAS åpnes ved å følge lenken til BVAS versjon 3 via (MD app). Skadeindeks (VDI). Vasculitis Damage Index (VDI) gjengir skader som er permanente, har vart minst tre måneder og ikke bedres av behandling. Skadene skal være forårsaket av ANCA-vaskulitt eller behandlingen. VDI-skår kan ikke avta, bare øke eller forbli stabil over tid. Alvorlig skade defineres som skår på 5 eller mer. Skader på øvre luftveier (Øre-Nese-bihuler-luftrør), hjerte og blodårer og nyrer er vanligst (referanse: Mohammad AJ, 2009). VDI kalkulator.
Behandling
Før behandlingen starter. Det er viktig å være oppklart om sykdommen, behandlingsmålet og om bivirkninger som kan oppstå. Sykdomsaktivitet og eventuell organskade registreres med tanke på senere sammenligning for å kunne vurdere effekt av behandlingen.
Infeksjonsrisiko øker under behandlingen. Andre årsaker til redusert immunforsvar kartlegges (sykehistorie, blodprøver med antall hvite blodlegemer, immunglobulin / IgG). Vaksiner for beskyttelse mot influensa og pneumokokker (lungebetennelse) kan være aktuelt i forkant av behandlingsstart, der tiden tillater det. Latente infeksjoner som Tuberkulose (Tbc), Hepatitt B og HIV utelukkes ved blodprøver.
Medikamentbehandlingen består av induksjonsbehandling og vedlikeholdsbehandling og er ofte ganske lik som annen ANCA-vaskulitt og Polyarteritis nodosa (PAN). Induksjonsbehandlingen skal få sykdommen under kontroll, noe som ofte tar noen måneder. Prednisolon eller Solu-Medrol (kortison intravenøst) er vanligvis ikke nok til å stanse sykdommen, slik at en kombinerer med andre legemidler. Vedlikeholdsbehandling kan vare flere år. Vennligst se separat side om behandling her.
Prognose
Sykdommen forløper ofte alvorlig, særlig før medikamentene får den under kontroll. Deretter forekommer tilbakefall, men risikoen er mindre enn ved GPA / Wegeners granulomatose. Viktig for en god prognose er: Tidlig diagnose og behandlingsstart, at behandlingen gjennomføres mot behandlingsmålet som planlagt og at infeksjoner forebygges, gjenkjennes og behandles.
Fire faktorer som kan øke alvorlighetsgraden («five factor score») (Referanse: Guillevin L, 2011)
- Alder over 65 år
- Kreatinin over 150 (redusert nyrefunksjon)
- Mage-tarm systemet er angrepet
- Hjertesykdom
Uten noen for for behandling med legemidler dør 90% i løpet av ett år. Med behandling er ett års overlevelse beregnet til 82% og 5 års overlevelse 76% når nyrene er angrepet (som gjelder de fleste). Varig nyresvikt utvikler seg hos 28%. I en norsk studie fra NOSVAR-registeret var dødeligheten lett økt sammenlignet med like gamle personer av samme kjønn uten ANCA-vaskulitt (Standard mortalitetsrate/SMR 1,5 som tilsier 1,5 ganger økt dødelighet) (Referanse Garen T, 2018). Blant gamle personer, 75 år og eldre med ANCA-vaskulitt er dødeligheten høyere, beregnet SMR er 3,69, hvorav størst risiko foreligger første året etter diagnosen med SMR 5,05 (referanse: Weiner M, 2015). Årsaker til død det første året fra diagnose er lungeblødning, nyresvikt og infeksjoner (referanse: Kallenberg CG, 2013).
Re-innleggelse i sykehus. De senere år er antall senger i sykehusene redusert kraftig. Behovet for innleggelse i sykehus er derfor viktig å evaluere. Spesielt er eldre personer utsatt for komplikasjoner som infeksjoner, nyre-svikt, hjerte- og karsykdommer og blodpropper etter diagnose og start av behandling. En svensk multisenter studie som omfattet fire svenske (Lund, Malmö, Linköping, Stockholm) og tre utenlandske sentra fra Tsjekkia (Prag) og England (London og Cambridge) evaluerte sykehus-opphold ved ANCA-vaskulitt (MPA 69,8%, GPA 30,2%) hos pasienter i alderen 75 år og eldre. Pasientene lå median 18 dager på sykehus initialt (diagnostisering og behandlings-start). Det første året etter diagnose ble 69,1% innlagt på ny av følgende hovedårsaker: Infeksjoner (37,2%), dialyse-relaterte problemer ved nyresvikt (11,5%), hjerte-kar sykdommer (9,6%), tilbakefall av ANCA-vaskulitt forelå bare hos 5,1%. I alt var pasientene innlagt i alt en måned (median 31 dager) på sykehus det første året av sykdommen. Resultatene viser at i en aldrende befolkning er sykehussenger fortsatt nødvendig for denne gruppen pasienter (Referanse: Weiner M, 2019).
Svangerskap ved MPA
Mikroskopisk polyangiitt (MPA) begynner oftest hos eldre personer. Data om svangerskap er derfor begrenset til relativt få tilfeller. Dersom sykdommen er behandlet og uten sykdomsaktivitet (i remisjon) og uten medikamenter før svangerskap, forventes ikke spesielle komplikasjoner for mor, foster eller nyfødt. Hvis sykdomsaktivitet, organ-manifestasjoner og nødvendig medikament-behandling er det økt risiko for komplikasjoner som omfatter pre-eklampsi («svangerskapsforgiftning»), spontanaborter, dødfødsler og nyre-komplikasjoner hos mor. Svangerskap ved MPA anbefales derfor fulgt opp som «risiko-svangerskap» (referanse: Pagnoux C, 2013; Pecher A-C, 2023). Vennligst les mer om svangerskap ved revmatisk sykdom på separat side.
Litteratur
- Jennette JC, 2017
- Yates M, 2016 (EULAR recommendations for management)
- Watts RA, 2012 (epidemiologi)
- Pecher A-C, 2023 (svangerskap)
- Chung SA, 2010
- Grans Kompendium i Revmatologi

